
【我們想讓你知道】
腦中風是造成全球人口死亡與失能的主要原因,黃金搶救時間僅3~4.5小時,而順藥的腦中風新藥若成功上市,治療的時間窗可延長至24小時,將是一大突破。
撰文:龔招健(資深投資達人)
台灣今(2024)年5月將迎來第一位醫師出身的新總統,接著7月將邁入生技月,部分有題材的國內生技股近期股價明顯加溫,其中,腦中風新藥二期臨床進入2b(此二期臨床分為2a、2b兩階段)、拚年底解盲的順藥(6535)走勢最為強勁,年初以來短短1個月就飆漲約1倍。
生技新藥股股價走勢跟其新藥潛力與臨床試驗進展息息相關。去年1月,順藥的缺血性腦中風新藥LT3001剛開始在美國、台灣、中國的醫學中心進行2b臨床試驗收案,當時股價僅40元上下,處於長線低檔區,本刊當時曾專文報導順藥將有機會成為長線大黑馬,今年1月初,股價上漲至68元左右,3月4號股價最高則來到188元,短短3個月,飆漲2.76倍。
延伸閱讀:順藥(6535)將成下一批新藥股黑馬?
順藥股價走勢
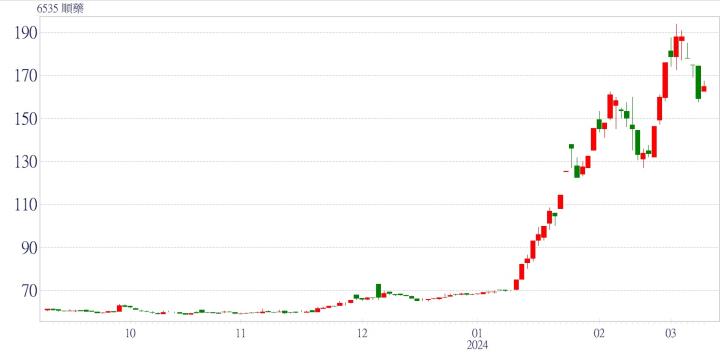
資料來源:CMoney法人投資決策系統,2023/09/08~2024/03/11
順藥是晟德(4123)集團旗下新藥開發主體事業,LT3001具有全新的活性成分,具溶血栓與神經保護(清除自由基)雙效潛能,目前已進入3個「多國多中心」(指我國與十大先進國至少一國,同步執行相同計劃編號的藥品臨床試驗)關鍵二期2b臨床試驗,包含單獨使用以及併用器械取栓之多劑量給藥設計。
其中,順藥主導的2個跨國(美國白人、台灣)2b臨床試驗,正加碼啟動歐洲區(白人)收案,以加速試驗進程。另一個由中國授權夥伴上海醫藥集團負責的中國區臨床試驗,則在收案啟動1年內就達到一半以上的收案人數,進展超乎預期,目標是今年底進行期末解盲,一旦解盲成功,將有機會成為世界級重磅新藥,搶攻全球每年2千億~3千億元台幣商機。
LT3001目標年底解盲 冀成世界級重磅新藥
順藥LT3001中國2b臨床試驗收案對象主要是中重度腦中風病患,占73%;美、台臨床試驗收案對象則為腦中風後4.5~24小時的病患,即目前唯一治療藥物tPA(血栓溶解劑)治療標準(3~4.5小時)以外的病人。其中,中國的2b臨床試驗進展最快,預計今年6、7月最後一個病人治療完成,解盲的數據可望在年底出爐。
全球每年約有1,500萬人中風,且每年約造成600萬人死亡,死亡率排名僅次於心臟冠狀動脈疾病和癌症,患者即使存活,通常會遺留下不同程度的神經功能障礙,是成年人和老人中重度肢體殘廢的主要原因之一。以台灣而言,腦中風居國人10大死因的前5名,平均每年奪走1萬多條寶貴的性命,尤其入冬後,隨著氣溫驟降,中風個案明顯增加。
中風大致可分為缺血性中風(或稱腦梗塞)、出血性中風(或稱腦出血),前者是國人最常見的中風型態。美國食品暨藥物管理局(FDA)於1996年核准的血栓溶解劑tPA,是第一個可有效治療腦梗塞的藥物,也是目前唯一被美國FDA、歐洲藥物管理局核准用於急性缺血性腦中風的藥物。
不過,tPA必須在患者腦梗塞發作3小時內(歐洲核准於4.5小時內使用),給予靜脈注射,才可將血塊溶解、疏通血管,這3~4.5小時是所謂的「黃金搶救時間」,一旦錯過就無藥可救。
另一方面,tPA在注射後有5%~10%的機率引發腦出血,加上3~4.5小時的使用時間限制與諸多禁忌(須排除最近顱內或體內出血、胃腸道潰瘍等因素),導致目前急性缺血性腦中風病患實際使用tPA的比率不到10%。
tPA是大分子蛋白藥,上市已20多年,至今仍無成功完成3期人體臨床的缺血性腦中風新藥開發案,這類中樞神經疾病的藥物開發難度顯然很高,順藥的LT3001被寄予厚望。
參與新藥開發經驗豐富的順藥董事長林榮錦表示,LT3001是結合短肽與小分子的全新活性成分新藥,相較於tPA,有量產製造上的優勢,且動物及人體臨床試驗皆證實其安全性,治療的時間窗更大幅拉長至24小時,「一旦開發成功,將取代tPA,且每年可治療的腦中風患者將是tPA的數倍,勢必成為全球矚目的重磅新藥,授權金可望超過10億美元,上市之後每年還會有更可觀的銷售分潤。」
取得FDA快速審查資格 有望推進國際授權進度
順藥2021年8月公布LT3001的2a人體臨床試驗(美國、台灣)解盲結果,達到試驗主要安全性指標,並顯示具有改善病患神經行為學的療效趨勢。LT3001在2022年初亦取得美國FDA「快速審查認定」,這有助於縮短審查時間,加速取得藥證。
「我認為LT3001的成功機率很大,將來不僅可救人,也讓很多家庭免於被拖垮。」林榮錦透露,有數家全球排名前10大的藥廠對這個新藥感興趣,跟順藥有初步接觸,預定今年底解盲的中國2b期末臨床試驗數據若達標,將進一步洽談授權事宜。
除了急性腦中風治療新藥,順藥也開發需求迫切卻未被滿足的腦神經損傷的修復與再生新療法,後者未來可銜接為腦中風患者的復健療法,甚至是治療其他目前尚無藥可醫的腦神經損傷、神經退化疾病,例如失智症(阿茲海默症占大宗)、巴金森氏症等。
投入幹細胞外泌體技術 深耕中樞神經領域藥物
為此順藥在前年6月引進國家衛生研究院的「誘導型幹細胞外泌體(iExo)之疾病治療技術」,並轉讓此技術至旗下的顥晟生醫(由順藥與晟德共同投資,分別持股6成、4成)。該技術已取得中華民國、美國專利,可自動化產出強化版外泌體,克服產量瓶頸,使幹細胞能大量分泌出含有促使腦神經再生之活性物質的外泌體。
外泌體是細胞吐出來的囊泡,直徑約40~160奈米,是細胞間的溝通工具。國家衛生研究院細胞與系統醫學研究所團隊歷經7年研究發現,利用特殊專利技術刺激間質幹細胞(廣泛存在於骨髓、脂肪裡),可分離出具有修復細胞功能的「幹細胞外泌體」,並從中鑑定出可促使腦神經再生及腦部功能恢復的物質,同時具有抗發炎、壓制過度免疫反應的功能。
美國FDA尚未核准以外泌體作為臨床治療的新藥上市,這類藥物最大的困難在於產品分離純化與擴大量產的技術壁壘,而晟德轉投資的聖安生醫(6926)專注於癌細胞靶向外泌體新藥開發,在這方面已有所突破,顥晟生醫因此在去年底自聖安技轉相關技術,雙方共同合作,以加速開發中樞神經領域的外泌體新藥。
順藥 小檔案(6535)
成立時間:2000年
資本額:16.5億元
董事長/總經理:林榮錦
營運項目:新藥開發
(圖片來源:ShutterStock,僅示意 / 內容僅供參考,投資請謹慎為上)
文章出處:《Money錢》2024年3月號
觀看更多內容,歡迎訂閱《Money錢》雜誌

 發表
發表


 我的網誌
我的網誌


